Kanker kolorektal nonpolyposis herediter (HNPCC), disebut juga Sindrom Lynch, adalah kondisi genetik dominan autosomal yang dikaitkan dengan risiko tinggi kanker usus besar serta kanker lainnya termasuk kanker endometrium (paling umum kedua), ovarium, lambung, usus kecil, saluran hepatobilier, saluran kemih bagian atas, otak, dan kulit. Peningkatan risiko kanker ini disebabkan oleh mutasi bawaan yang merusak perbaikan ketidakcocokan DNA. Ini adalah jenis sindrom kanker.
Gejala sindrom Lynch
Risiko kanker
Risiko seumur hidup dan usia rata-rata saat diagnosis untuk kanker terkait sindrom Lynch
| Jenis kanker | Risiko seumur hidup (%) | Usia rata-rata saat diagnosis (tahun) |
| Kolorektal | 52-58 | 44-61 |
| Endometrium | 25-60 | 48-62 |
| Lambung | 6-13 | 56 |
| Ovarium | 4-12 | 42.5 |
Selain jenis kanker yang terdapat pada bagan di atas, dapat dipahami bahwa sindrom Lynch juga berkontribusi terhadap peningkatan risiko kanker usus halus, kanker pankreas, kanker ureter / pelvis ginjal, kanker saluran empedu, kanker otak, dan neoplasma sebasea. Peningkatan risiko kanker prostat dan kanker payudara juga dikaitkan dengan sindrom Lynch, meskipun hubungan ini tidak sepenuhnya dipahami.
Dua pertiga dari kanker usus besar terjadi di usus besar proksimal dan tanda dan gejala umum termasuk darah dalam tinja, diare atau sembelit, dan penurunan berat badan yang tidak diinginkan. Usia rata-rata diagnosis kanker kolorektal adalah 44 tahun untuk anggota keluarga yang memenuhi kriteria Amsterdam. Usia rata-rata diagnosis kanker endometrium adalah sekitar 46 tahun. Di antara wanita dengan HNPCC yang memiliki usus besar dan kanker endometrium, sekitar setengahnya datang pertama kali dengan kanker endometrium, menjadikan kanker endometrium sebagai kanker sentinel paling umum pada sindrom Lynch. Gejala kanker endometrium yang paling umum adalah perdarahan vagina yang tidak normal. Pada HNPCC, usia rata-rata diagnosis kanker lambung adalah 56 tahun dengan adenokarsinoma tipe usus menjadi patologi yang paling sering dilaporkan. Kanker ovarium terkait HNPCC memiliki usia rata-rata diagnosis 42,5 tahun; sekitar 30% didiagnosis sebelum usia 40 tahun.
Variasi yang signifikan dalam tingkat kanker telah ditemukan tergantung pada mutasi yang terlibat. Sampai dengan usia 75 tahun risiko kanker kolorektal, kanker endometrium, kanker ovarium, gastrointestinal bagian atas (lambung, duodenum, saluran empedu atau pankreas), kanker saluran kemih, kanker prostat dan tumor otak adalah sebagai berikut: untuk mutasi MLH1 risiko adalah 46%, 43%, 10%, 21%, 8%, 17% dan 1% masing-masing; untuk mutasi MSH2 risikonya masing-masing 57%, 17%, 10%, 25%, 32%, dan 5%; untuk mutasi MSH6 risikonya masing-masing adalah 15%, 46%, 13%, 7%, 11%, 18% dan 1%.
| Gen | Risiko kanker ovarium | Risiko kanker endometrium |
|---|---|---|
| MLH1 | 4-24% | 25-60% |
| MSH2 / EPCAM | 4-24% | 25-60% |
| MSH6 | 1-11% | 16-26% |
| PMS2 | 6% (risiko gabungan) | 15% |
Genetika

HNPCC diturunkan secara autosom dominan. Ciri khas HNPCC adalah perbaikan ketidaksesuaian DNA yang rusak, yang menyebabkan peningkatan laju perubahan nukleotida tunggal dan ketidakstabilan mikrosatelit, juga dikenal sebagai MSI-H (H adalah “tinggi”). MSI dapat diidentifikasi dalam spesimen kanker di laboratorium patologi. Sebagian besar kasus mengakibatkan perubahan panjang pengulangan dinukleotida dari nukleobase sitosin dan adenin (urutan: CACACACACA…).
4 gen utama yang terlibat dalam HNPCC biasanya menyandikan protein yang membentuk dimer untuk berfungsi:
- Protein MLH1 dimerisasi dengan protein PMS2 untuk membentuk MutLα, yang mengoordinasikan pengikatan protein lain yang terlibat dengan perbaikan ketidakcocokan seperti DNA helicase, single-stranded-DNA binding-protein (RPA), dan DNA polimerase.
- Protein MSH2 dimerisasi dengan protein MSH6, yang mengidentifikasi ketidaksesuaian melalui model penjepit geser, protein untuk memindai kesalahan.
Kerusakan salah satu gen untuk dimer protein merusak fungsi protein. Keempat gen ini terlibat dalam koreksi kesalahan (mismatch repair), sehingga disfungsi gen tersebut dapat mengakibatkan ketidakmampuan untuk memperbaiki kesalahan replikasi DNA dan menyebabkan HNPCC. HNPCC diketahui terkait dengan mutasi lain pada gen yang terlibat dalam jalur perbaikan ketidakcocokan DNA:
| Nama OMIM | Gen yang terlibat dalam HNPCC | Frekuensi mutasi pada keluarga HNPCC | Tempat | Publikasi pertama |
|---|---|---|---|---|
| HNPCC1 (120435) | MSH2 / EPCAM | sekitar 60% | 2p22 | Fishel 1993 |
| HNPCC2 (609310) | MLH1 | sekitar 30% | 3p21 | Papadopoulos 1994 |
| HNPCC5 | MSH6 | 7-10% | 2p16 | Miyaki 1997 |
| HNPCC4 | PMS2 | relatif jarang | 7p22 | Nicolaides 1994 |
| HNPCC3 | PMS1 | laporan kasus | 2q31-q33 | Nicolaides 1994 |
| HNPCC6 | TGFBR2 | laporan kasus | 3p22 | |
| HNPCC7 | MLH3 | diperdebatkan | 14q24.3 |
Kebanyakan penderita HNPCC mewarisi kondisi tersebut dari orang tua. Namun, karena penetrasi yang tidak lengkap, diagnosis kanker yang bervariasi, pengurangan risiko kanker, atau kematian dini, tidak semua orang dengan mutasi gen HNPCC memiliki orang tua yang menderita kanker. Beberapa orang mengembangkan HNPCC de-novo dalam generasi baru, tanpa mewarisi gen. Orang-orang ini sering hanya diidentifikasi setelah mengembangkan kanker usus besar pada masa awal kehidupan. Orang tua dengan HNPCC memiliki peluang 50% untuk meneruskan mutasi genetik ke setiap anak. Penting juga untuk dicatat, bahwa mutasi yang merusak pada salah satu gen MMR saja tidak cukup untuk menyebabkan kanker, tetapi mutasi lebih lanjut pada gen penekan tumor lainnya perlu terjadi.
Diagnosis sindrom Lynch
Diagnosis sindrom Lynch diterapkan pada orang dengan mutasi DNA germline di salah satu gen MMR (MLH1, MSH2, MSH6, dan PMS2) atau gen EPCAM, yang diidentifikasi dengan pengujian genetik. Kandidat untuk pengujian genetik germline dapat diidentifikasi dengan kriteria klinis seperti Amsterdam Clinical Criteria dan Bethesda Guidelines, atau melalui analisis tumor dengan imunohistokimia (IHC), atau pengujian ketidakstabilan mikrosatelit (MSI). Di AS, perkumpulan profesional merekomendasikan pengujian setiap kanker usus besar untuk MSI atau IHC sebagai skrining untuk sindrom Lynch, tetapi ini tidak selalu dilakukan karena keterbatasan biaya dan sumber daya. Tes genetik tersedia secara komersial dan terdiri dari tes darah.
Imunohistokimia
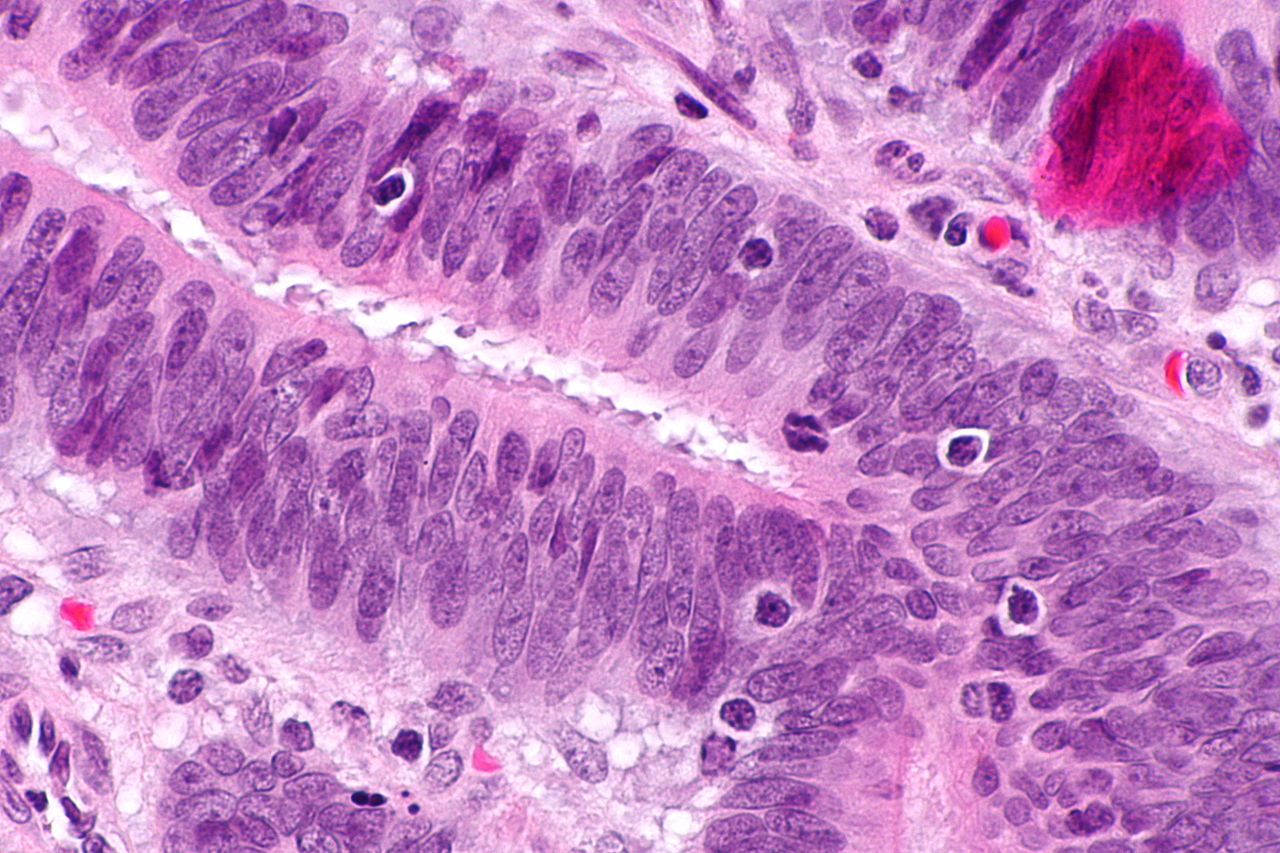
Immunohistochemistry (IHC) adalah metode yang dapat digunakan untuk mendeteksi ekspresi protein abnormal mismatch repair (MMR) pada tumor yang berhubungan dengan sindrom Lynch. Meskipun bukan diagnosis sindrom Lynch, ini dapat berperan dalam mengidentifikasi orang yang harus menjalani pengujian germline. Dua metode pelaksanaan pengujian IHC meliputi pengujian berbasis usia dan pengujian universal untuk semua orang. Saat ini, tidak ada kesepakatan luas mengenai metode skrining mana yang harus digunakan. Pengujian berbasis usia untuk IHC telah disarankan sebagian karena analisis biaya-manfaat, sedangkan pengujian universal untuk semua orang dengan kanker kolorektal memastikan orang dengan sindrom Lynch tidak terlewatkan. Untuk mengatasi biaya, para peneliti mencoba memprediksi MSI atau IHC secara langsung dari tampilan tumor di bawah mikroskop, tanpa melakukan pengujian molekuler.
Ketidakstabilan Mikrosatelit
Mutasi pada sistem perbaikan ketidakcocokan DNA dapat menyebabkan kesulitan transmisi daerah di dalam DNA yang mengandung pola berulang dari dua atau tiga nukleotida (mikrosatelit), atau dikenal sebagai ketidakstabilan mikrosatelit (MSI). MSI diidentifikasi melalui ekstraksi DNA dari sampel jaringan tumor dan sampel jaringan normal diikuti dengan analisis PCR dari daerah mikrosatelit. Analisis MSI dapat digunakan untuk mengidentifikasi orang yang mungkin memiliki sindrom Lynch dan mengarahkan mereka untuk pengujian lebih lanjut.
Klasifikasi
Tiga kelompok utama kanker MSI-H (ketidakstabilan mikrosatelit – MSI) dapat dikenali dari kriteria histopatologi:
- kanker sisi kanan berdiferensiasi buruk
- kanker musinous sisi kanan
- adenokarsinoma di lokasi mana pun yang menunjukkan tingkat limfosit intraepitel (TIL) yang dapat diukur
Kriteria histopatologi tidak cukup sensitif untuk mendeteksi MSI dari histologi tetapi peneliti mencoba menggunakan kecerdasan buatan untuk memprediksi MSI dari histologi.
Selain itu, HNPCC dapat dibagi menjadi sindrom Lynch I (kanker usus besar keluarga) dan sindrom Lynch II (HNPCC yang terkait dengan kanker saluran cerna atau sistem reproduksi lainnya).
Pencegahan
Tes seleksi
Konseling genetik dan pengujian genetik direkomendasikan untuk keluarga yang memenuhi kriteria Amsterdam, sebaiknya sebelum timbulnya kanker usus besar.
Kanker usus besar
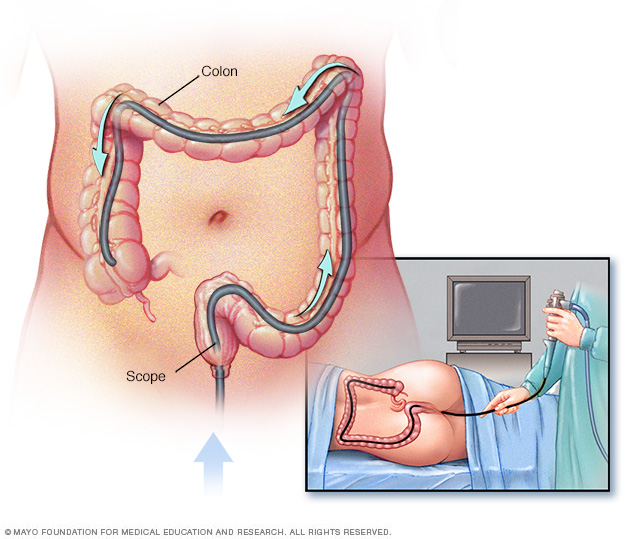
Kolonoskopi direkomendasikan sebagai metode surveilans pencegahan untuk individu yang memiliki sindrom Lynch, atau gen terkait LS. Secara khusus, direkomendasikan bahwa kolonoskopi dimulai pada usia 20-25 untuk pembawa mutasi MLH1 dan MSH2 dan 35 tahun untuk pembawa mutasi MSH6 dan PMS2. Surveilans kolonoskopi kemudian harus dilakukan dengan interval 1-2 tahun untuk pasien sindrom Lynch.
Kanker endometrium / ovarium
USG transvaginal dengan atau tanpa biopsi endometrium direkomendasikan setiap tahun untuk skrining kanker ovarium dan endometrium. Untuk wanita dengan sindrom Lynch, tes darah CA-125 tahunan dapat digunakan untuk menyaring kanker ovarium, namun data tentang kemanjuran tes ini dalam mengurangi kematian masih terbatas.
Kanker lainnya
Ada juga strategi untuk mendeteksi kanker lain lebih awal atau mengurangi kemungkinan mengembangkannya yang dapat didiskusikan oleh orang dengan sindrom Lynch dengan dokter mereka, namun keefektifannya tidak jelas. Opsi-opsi ini meliputi:
- Endoskopi bagian atas untuk mendeteksi kanker perut dan usus halus setiap 3–5 tahun, dimulai pada usia 30 paling awal (sebaiknya dalam pengaturan penelitian)
- Urinalisis tahunan untuk mendeteksi kanker kandung kemih, dimulai pada usia 30 paling awal (sebaiknya dalam pengaturan penelitian)
- Ujian fisik dan neurologis tahunan untuk mendeteksi kanker di sistem saraf pusat (otak atau sumsum tulang belakang), dimulai pada usia 25 paling awal
Kriteria Amsterdam
Berikut ini adalah kriteria Amsterdam dalam mengidentifikasi kandidat berisiko tinggi untuk pengujian genetik molekuler:
Kriteria Amsterdam I (semua poin peluru harus dipenuhi):
- Tiga atau lebih anggota keluarga dengan diagnosis pasti kanker kolorektal, salah satunya adalah kerabat tingkat pertama (orang tua, anak, saudara kandung) dari dua lainnya
- Dua generasi yang terpengaruh berturut-turut
- Satu atau lebih kanker usus besar didiagnosis di bawah usia 50 tahun
- Poliposis adenomatosa familial (FAP) telah disingkirkan
Kriteria Amsterdam II dikembangkan pada tahun 1999 dan meningkatkan sensitivitas diagnostik untuk sindrom Lynch dengan memasukkan kanker endometrium, usus halus, ureter, dan pelvis ginjal.
Kriteria Amsterdam II (semua poin peluru harus dipenuhi):
- Tiga atau lebih anggota keluarga dengan kanker terkait HNPCC, salah satunya adalah kerabat tingkat pertama dari dua lainnya
- Dua generasi yang terpengaruh berturut-turut
- Satu atau lebih kanker terkait HNPCC yang didiagnosis di bawah usia 50 tahun
- Poliposis adenomatosa familial (FAP) telah disingkirkan
Pembedahan
Histerektomi profilaksis dan salpingo-ooforektomi (pengangkatan rahim, saluran telur, dan ovarium untuk mencegah berkembangnya kanker) dapat dilakukan sebelum kanker ovarium atau endometrium berkembang.
Pengobatan sindrom Lynch
Pembedahan tetap menjadi terapi garis depan untuk HNPCC. Pasien dengan sindrom Lynch yang mengembangkan kanker kolorektal dapat diobati dengan kolektomi parsial atau kolektomi total dengan anastomosis ileorektal. Karena peningkatan risiko kanker kolorektal setelah kolektomi parsial dan kualitas hidup yang serupa setelah kedua operasi, kolektomi total mungkin menjadi pengobatan pilihan untuk HNPCC, terutama pada pasien yang lebih muda.
Ada kontroversi yang sedang berlangsung mengenai manfaat terapi adjuvan berbasis 5-fluorouracil untuk tumor kolorektal terkait HNPCC, terutama pada stadium I dan II.
- Terapi antibodi anti-PD-1 bisa efektif.
Blokade pos pemeriksaan dengan terapi anti-PD-1 sekarang lebih disukai sebagai terapi lini pertama untuk Mikrosatelit-Instabilitas-Kanker kolorektal tingkat lanjut.
.













Discussion about this post